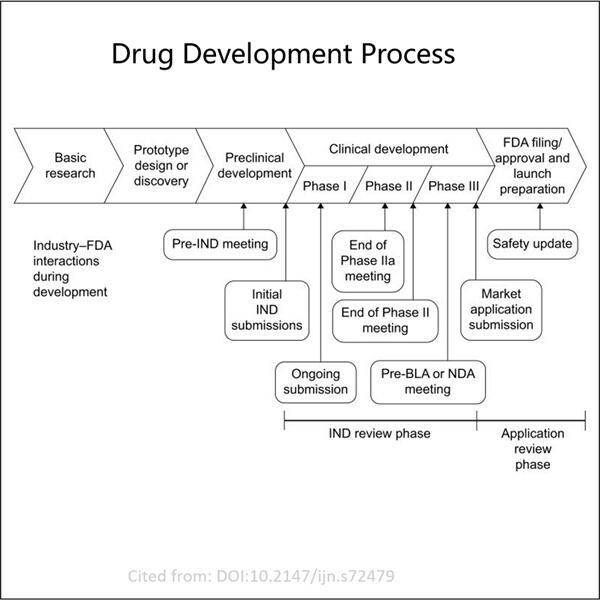
Јаохай знае многу за планинската медицина. Тие развијаа два вида на важни aplikacii-IND (indole) и BLA (blubber). IND е скратено за Investigational New Drug, користен за да се добие дозвола од АМС САД да се тестира нов лек на луѓето. Биолошкиот Лиценз за Прилагане (BLA) е неопходен кога компанија сака да продава биолошки производ. GMP Semaglutide API прикачени. Овие aplikacii се клучни чекори за да се осигури дека новите лекови се безбедни и ефикасни за луѓето. Во овој чланок ќе разговараме како да се приложат овие два вида aplikacii и нивните разлики како и сличности.
Фирмата што сака да поднесе барање за IND прво мора да поднесе специјално барање до Управата за храна и лекови (FDA). Ова е доста неопходно, бидејќи ќе содржи целитеessential детали за овој најнов лек. Барањето сега ќе оди пред FDA за разгледување, додека фирмата бара дозвола да започне тестирање на лекот во човеките. Ова дел од процесот обично трaje до 30 дена. Во втор ред, еднаш кога недостаснавајќите информации се поднесени и прифатени од страна на FDA - ако барањето биде прифатено - фирмата може да започне тестовите на човеките, што е голем корак кон креирање на нов лек.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN