Aanpassing, Efficiëntie & Kosteneffectiviteit
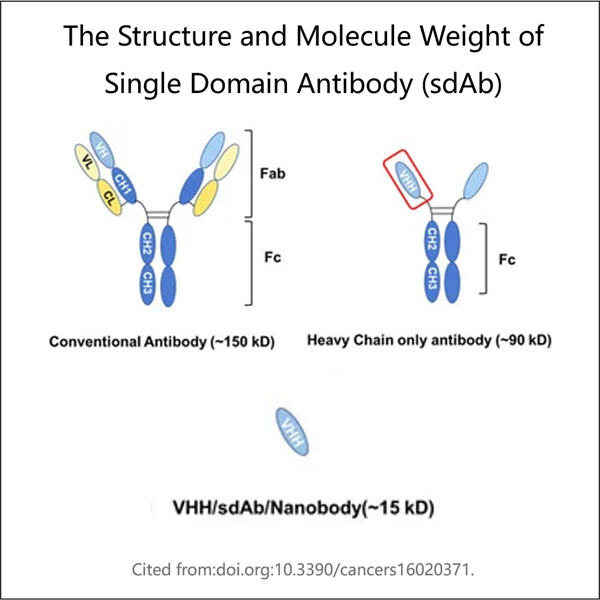
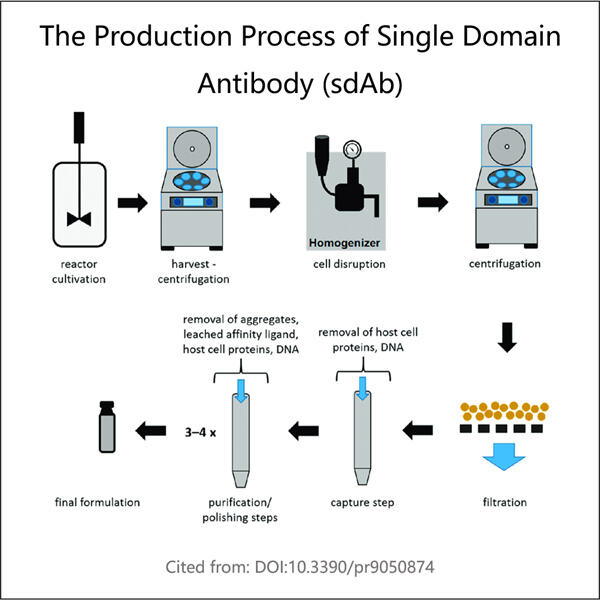
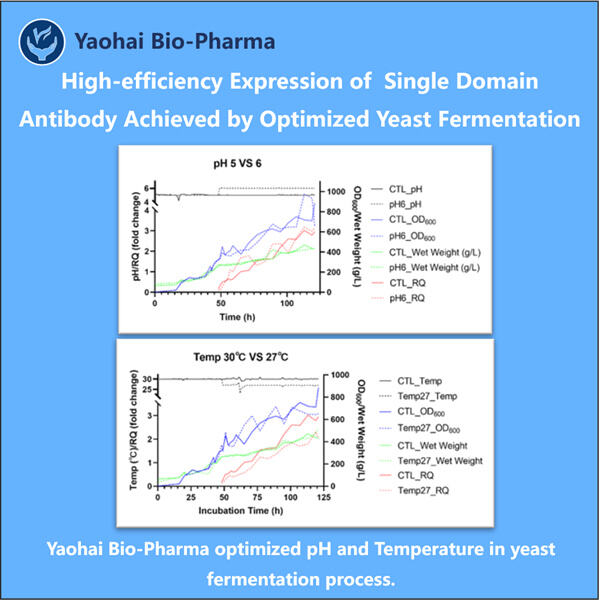
Yaohai Bio-Pharma is gespecialiseerd in procesontwikkeling van Single Domain Antibodies (sdAb) in microbieel afgeleide biologische producten. We bieden op maat gemaakte onderzoeks- en ontwikkelingsdiensten (RD) en productieoplossingen, terwijl we de risico's minimaliseren. We hebben meegewerkt aan verschillende modaliteiten zoals recombinante sub-eenheid vaccins, peptiden hormonen, cytostatische groeifactoren, single-domain antilichamen, enzymen, plasmid DNA, mRNA en andere. We zijn experts in verschillende microbiele gastheren, zoals gist (extracellulair en intracellulair, oplevering tot 15 gram per liter), bacteriële periplasma-secretie en oplosbare intracellulaire inclusiecorpora (oplevering tot 10 gram/L). Bovendien hebben we een BSL-2 microbiele fermentatieplatform ontwikkeld voor de ontwikkeling van bacteriële vaccins. We hebben een trackrecord van het verbeteren van productieprocessen, waardoor de opbrengst toeneemt en kosten dalen. Met een hoogwaardig technisch team garanderen we snelle en betrouwbare projectaflevering en brengen uw producten sneller naar de markt.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN