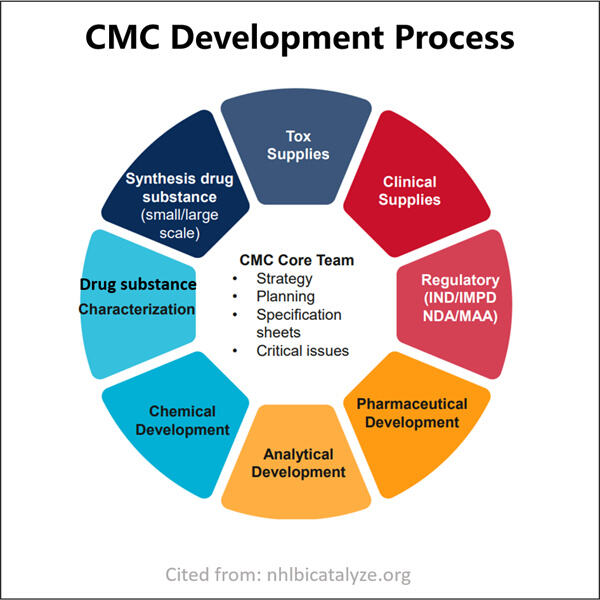
Navegasie deur die Tegniese Eise van Geneesmiddel Aanvrae
Dit is omdat een van die voorste basiese standpunte van stilte goedgekeur het bewys dat die item suiwer is en betroubare doeltreffendheid het. So, die metode van die vervaardiging van die gene moet streng gereg deur wat hoekom 'n paar stilte maatskappye met bykans vergelykbare s593 variasie saamgewerk het vir meer as 'n dekade om geneesmiddels te lewer. Dit sluit in dat die maatskappye deur 'n stap-vir-stap proses moet gaan om seker te maak dat die eindprodukt ook gehou word by hoë kwaliteitstandaarde. Dit kan fundamenteel wees aangesien mense se lewens in gevaar is van die gene wat hulle verbruik.
Maatskappye wat 'n geneesmiddel-aanvraag inskryf, moet data voorsien oor wat in die farmasie gaan en hoe dit gemaak word. Dit sluit die chemiese samestelling, vervaardigingsproses en veiligheidsparameters in wat daarin ingesluit is. Hierdie data word ook ondersteun deur wetenskaplike bewyse - wat illustreer dat die farmasie sowel veilig as doeltreffend is. Hoe beter die FDA dit kan verstaan, mRNA Gelyktydige Transkripsie en Kopving Protokol geneesmiddel, hoe groter die kans dat hulle sy inligting teenoor wat in ander studies gebruik is (meta-analise) kan vergelyk.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN