Com a aplicação ampla de vacinas de mRNA contra a COVID-19 em grandes populações, a segurança das vacinas de mRNA foi validada. O mRNA possui a capacidade de expressar qualquer proteína, oferecendo soluções potenciais para várias necessidades clínicas não atendidas.
A Yaohai Bio-Pharma fornece uma solução abrangente para o desenvolvimento de mRNA e a produção GMP, apoiada por uma plataforma de pesquisa robusta e um sistema GMP conforme. Nossos serviços são adaptados para atender às exigências únicas de nossos clientes, oferecendo-lhes substâncias farmacêuticas de alta qualidade baseadas em mRNA e produtos finais LNP-mRNA em quantidades de miligrama a grama, além de relatórios detalhados de desenvolvimento e produção e relatórios de testes.
Obtivemos autorização para a tecnologia patenteada de LNP de nosso parceiro, NanoStar Pharmaceuticals, garantindo evitar disputas potenciais de patentes no futuro.
solução Completa de mRNA/LNP da Yaohai Bio-Pharma
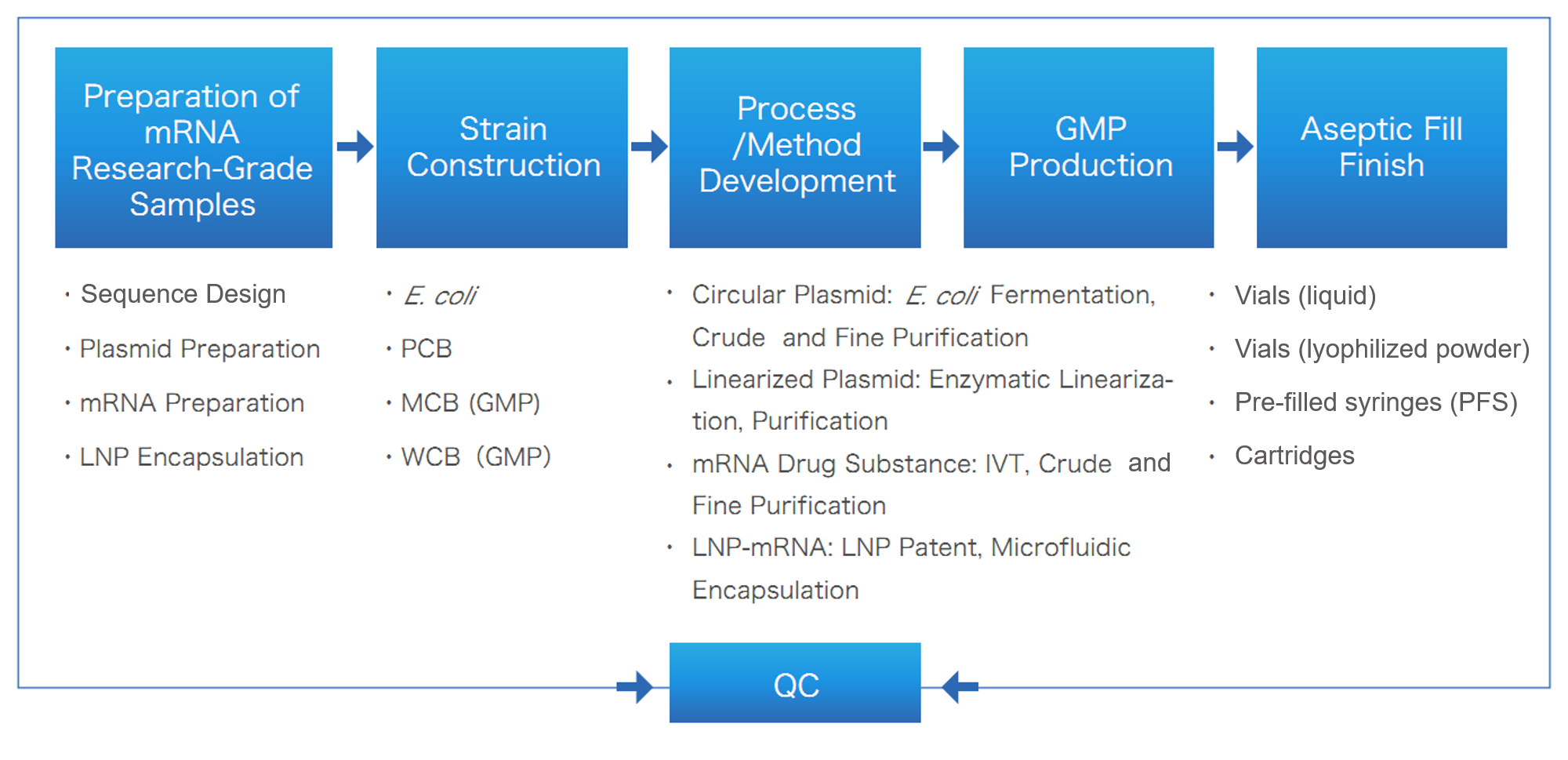
Entregáveis
| Grau |
Entregáveis |
Especificações |
Aplicações |
| não-GMP |
Substância Medicamentosa, mRNA |
0,1~10 mg (mRNA) |
Pesquisa pré-clínica, como transfeção celular, Desenvolvimento de métodos analíticos, Estudos pré-estabilidade, Desenvolvimento de formulação |
| Produto Farmacêutico, LNP-mRNA |
| GMP, Estéril |
Substância Medicamentosa, mRNA |
10 mg~70 g |
Investigational new drug (IND), Autorização de ensaio clínico (CTA), Suprimento para ensaios clínicos, Biologic license application (BLA), Suprimento comercial |
| Produto Farmacêutico, LNP-mRNA |
5000 frascos ou seringas/cartridge pré-enchidos |
Serviço CRDMO de mRNA da Yaohai, cobrindo o ciclo de vida inteiro do mRNA
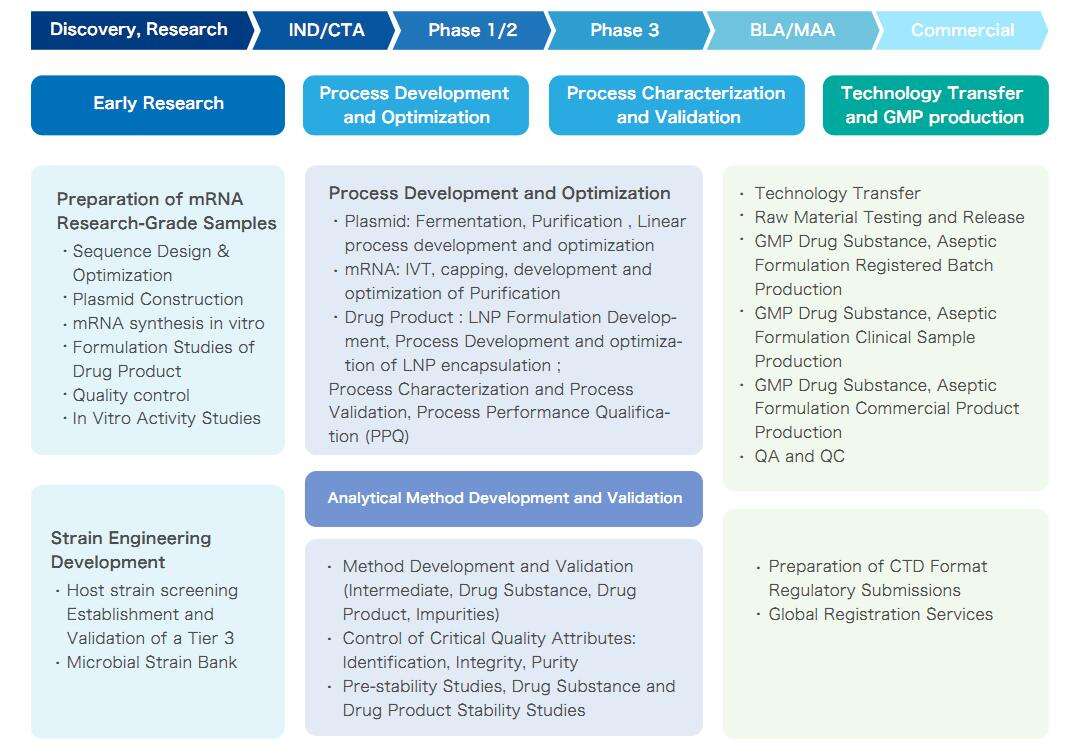
Recursos da Plataforma
Plataforma de DNA de Plasmídeo
- Múltiplos sistemas de fermentação de 7L, sem produtos de origem animal em todo o processo
- Rastreabilidade clara de plasmídeos e bactérias hospedeiras, sem obstáculos na declaração
- A produtividade de Plasmídeo contendo poli A excede 500 mg/L
- Taxa de perda de poli A inferior a 5 pb
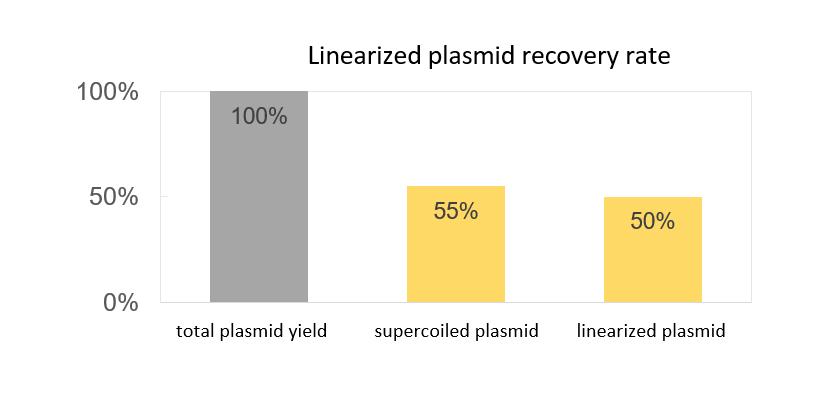
- Proporção de plasmídeo superenrolado maior que 90%; taxa de recuperação superior a 55%
- Eficiência de linearização superior a 99%; taxa de recuperação de plasmídeo linearizado de 90%
Plataforma de substância medicinal de mRNA
- Múltiplos Reatores de 1L (GMP)
- Uma alta taxa de transcrição de 1:120 permite um processo de IVT escalável
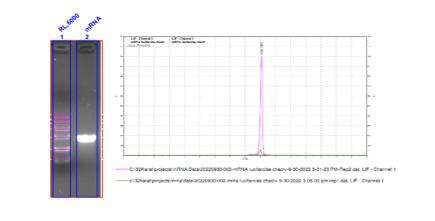
- integridade do mRNA excedendo 98%
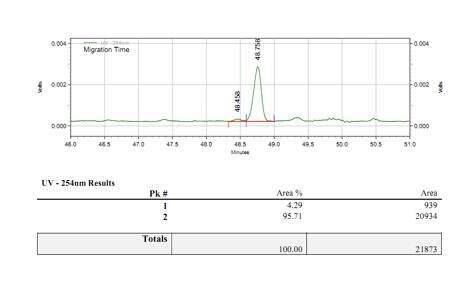
- Processo estável de capping com uma taxa de capping superior a 95%
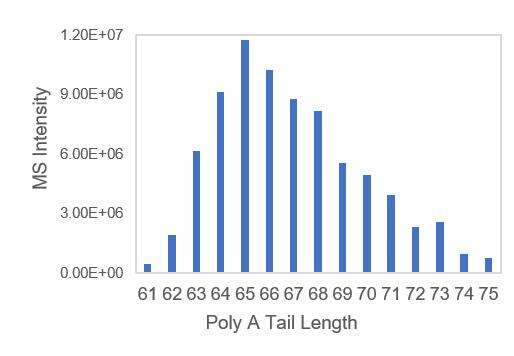
- Modelos de transcrição com caudas de A, garantindo distribuição uniforme de caudas poli-A.
Plataforma de Encapsulamento LNP
- Tecnologia de patente LNP autorizada por nossos parceiros para garantir a evitar disputas de patentes para nossos clientes.



(Nossos parceiros)
- Utilizando um processo versátil de encapsulamento microfluídico, alcançando uma eficiência de encapsulamento superior a 95%.
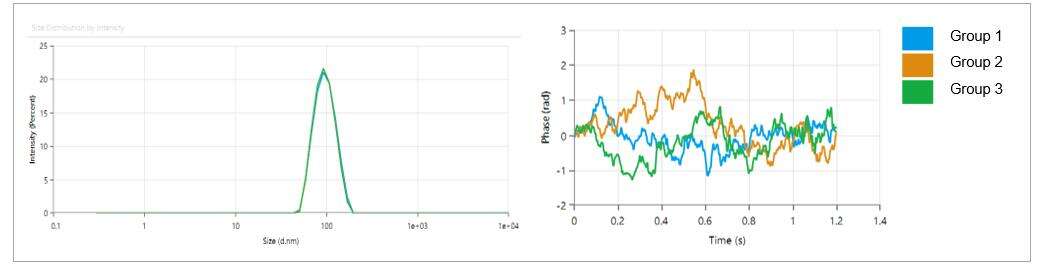
- O tamanho das partículas LNP está entre 80-100 nm, com um baixo índice de polidispersidade (PDI) de 0,05, indicando uma distribuição uniforme de tamanhos de partículas.
- As partículas LNP apresentam carga fraca, com potencial Zeta de aproximadamente -2,18 mV.
| Item de Teste |
Método de teste |
Resultado do Teste |
| Eficiência de Encapsulamento |
Ribogreen |
92,7% |
| Tamanho de Partícula |
Malvern |
92,07 nm |
| PDI |
Malvern |
0.05 |
| Zeta |
Malvern |
-2,18 mV |
Plataforma de Desenvolvimento de Método
Oferecemos uma plataforma abrangente de desenvolvimento de métodos para analisar plasmídeos circulares e linearizados, matérias-primas de mRNA e produtos finais de LNP-mRNA. Nossa análise cobre uma variedade de parâmetros, como integridade, pureza, eficiência de capping, distribuição de poli A, eficiência de encapsulamento, tamanho de partículas, componentes de LNP e vários resíduos do processo (HCP, HCD, HCR, dsRNA, antibióticos, DNase I, polimerase T7 RNA, enzima de capping da vacina, 2-O metiltransferase, etc.).
Métodos parciais são demonstrados da seguinte forma:
Detecção da Integridade do mRNA (Eletroforese em Capilar)
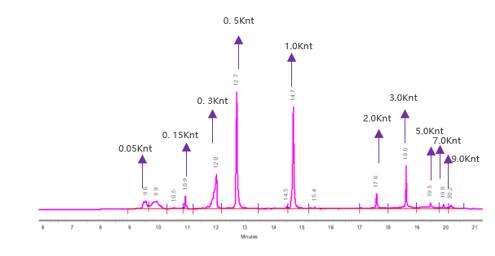
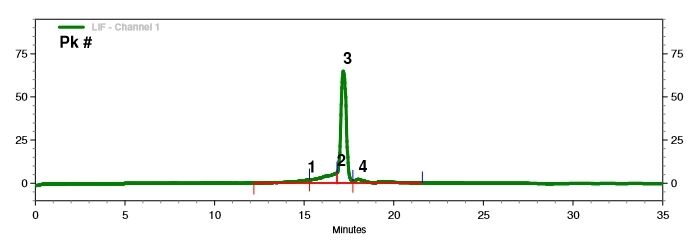
Desenvolvemos condições de separação ótimas para separar precisamente moléculas de mRNA de comprimentos variados.
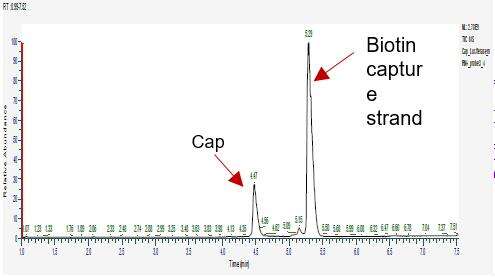
Detecção da Eficiência de Capping do mRNA (LC-MS)
Desenvolvemos condições adequadas para o corte e separação dos oligonucleotídeos da extremidade 5', permitindo a separação precisa de fragmentos capped e uncapped.
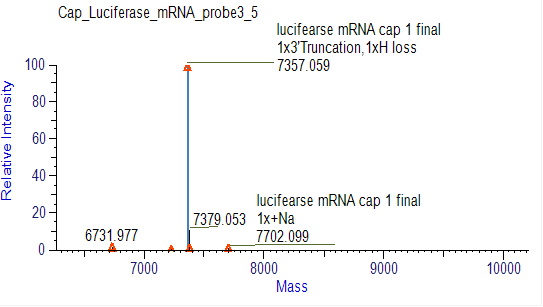
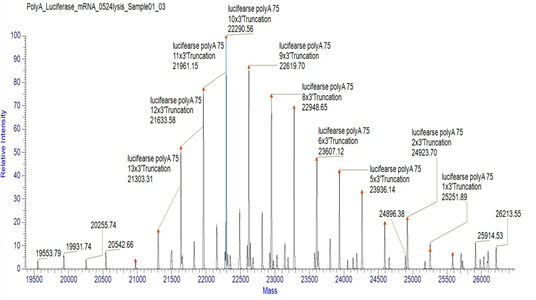
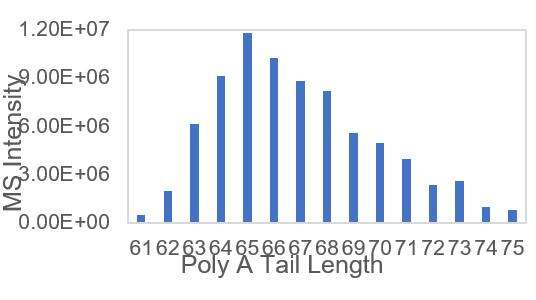
Detecção da Distribuição da Cauda PolyA do mRNA Adequada (LC-MS)
Desenvolvemos condições adequadas para o corte das extremidades 3' e separação dos oligonucleotídeos da extremidade 3', que permitem a detecção precisa da distribuição das caudas polyA.
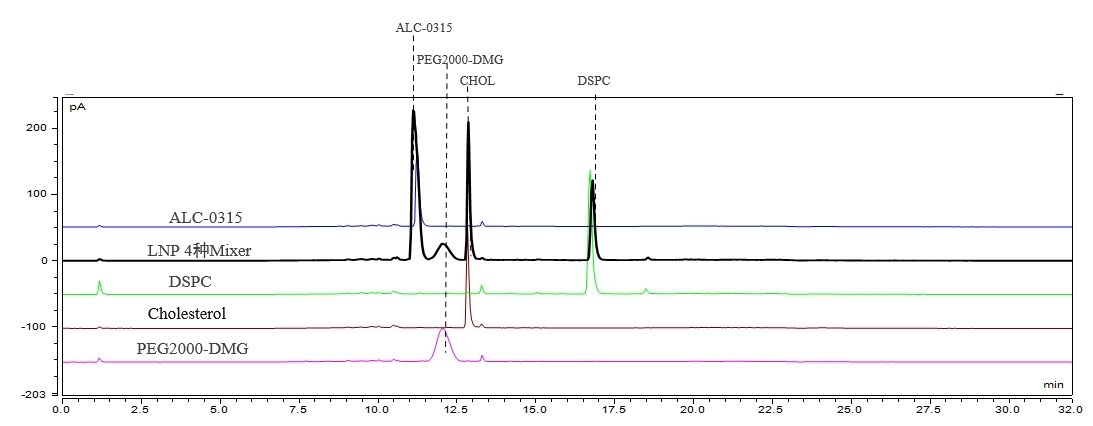
Detecção de Componentes e Conteúdo do LNP (HPLC-CAD)
Estabelecemos um método cromatográfico adequado que alcança a separação na linha de base de quatro componentes do LNP. Este método demonstra excelente reprodutibilidade.
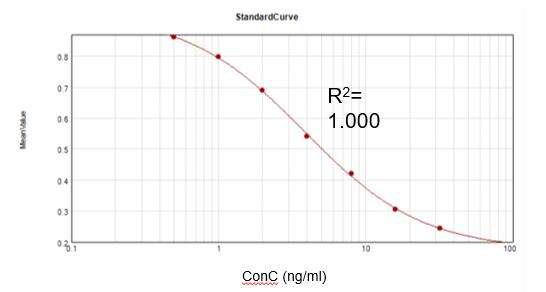
Concentração Residual de Kanamicina (ELISA)
Com base em um kit de ensaio comercial, obtivemos uma curva de calibração adequada (R2 = 1,000) e alcançamos uma taxa de recuperação de 104,8%.
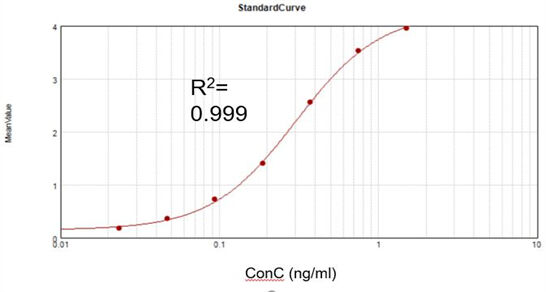
Concentração Residual de dsRNA
Com base em um kit de ensaio comercial, obtivemos uma curva de calibração ajustada adequada (R2 = 0,999) e alcançamos uma taxa de recuperação de 105,5%.
Resíduo de Polimerase RNA T7 (Elisa)
Com base em um kit de ensaio comercial, obtivemos uma curva de calibração ajustada adequada (R2 = 1,000) e alcançamos uma taxa de recuperação de 107,9%.
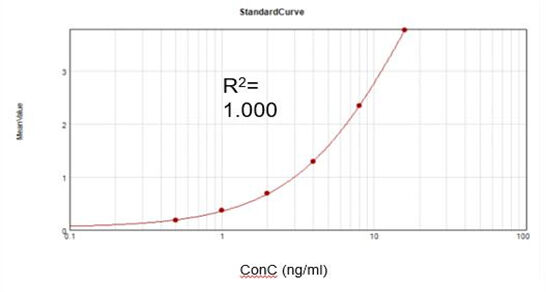
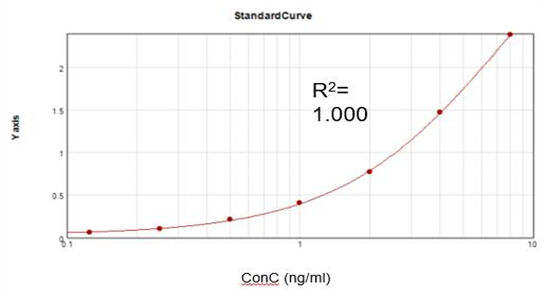
Resíduo da Enzima de Capping do Vírus Vaccinia (ELISA)
Com base em um kit de ensaio comercial, obtivemos uma curva de calibração ajustada adequada (R2 = 1,000) e alcançamos uma taxa de recuperação de 92%.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN






















