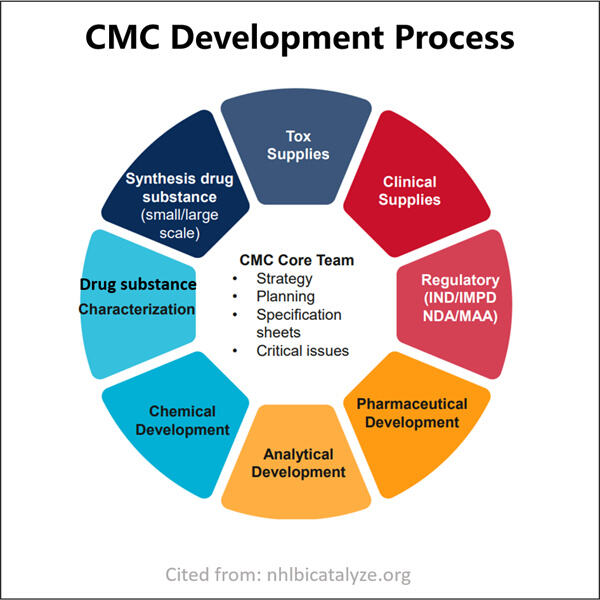
CMC står för Kemi, Fabrikation & Kontroll. Denna komponent kan vara en viktig del av den lugnande ansökningshanteringen för ett nytt läkemedel. Den berättar hur läkemedlet tillverkas och hur det har testats för att vara helt säker på att det är ett säkert, högkvalitativt medicinskt alternativ för de som ska ta detta preparat. Förståelse av vad Yaohai CMC Explanation innebär mRNA Kapningseffektivitetstestning för Plasmid DNA kan hjälpa till att ge en ny uppfattning om hur företag garanterar kvaliteten på sina produkter.
Det finns noggranna regler för att erbjuda ett läkemedel, företag måste visa att läkemedlet är väl konstruerat och bra för dig. FDA, som är förkortningen för Livsmedels- och Läkemedelsverket, innehåller en handledning om hur man förbereder och skickar in ansökningar för läkemedelsgodkännande. Reglerna skyddar hälsan hos både allmänheten och garanterar att endast säkra läkemedel är tillgängliga.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN