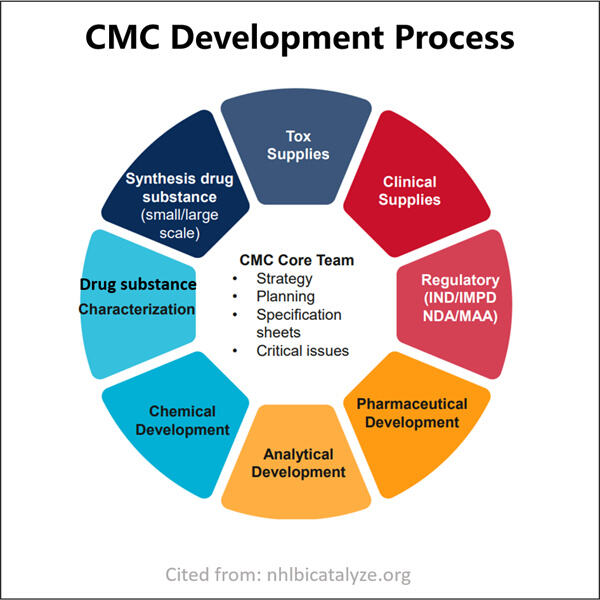
Penyesuaian, Kecekapan & Kos-Padu
Yaohai Bio-Pharma berpengalaman dalam produk biologi yang berasal dari sumber mikroba. Kami menyediakan penyelesaian RD tersuai dan pembuatan, sambil meminimumkan risiko yang mungkin berlaku. Kami telah bekerja pada pelbagai modali, termasuk vaksin subunit rekombinan, hormon peptida, sitokina faktor pertumbuhan, antibodi single-domain enzim, DNA plasmid mRNA pelbagai, dan lain-lain. Kami telah berspecialisasi dalam pelbagai mikroorganisma, termasuk seksyen CMC dalam permohonan ubat sekretori intrasel dan luar sel (keluaran hingga 15g/L) dan bakteria larutan intrasel dan badan inklusi (keluaran hingga 10g/L). Kami juga telah membina platform fermentasi BSL-2 untuk mencipta vaksin berasaskan bakteria. Kami adalah pakar dalam membaiki proses, meningkatkan hasil produk, dan menurunkan kos pengeluaran. Kami mempunyai pasukan teknologi yang sangat cekap yang memastikan penghantaran projek tepat masa dan berkualiti tinggi. Ini membolehkan kami membawa produk unik anda lebih pantas ke pasaran.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN