Experțise profesioniste și experiență vastă
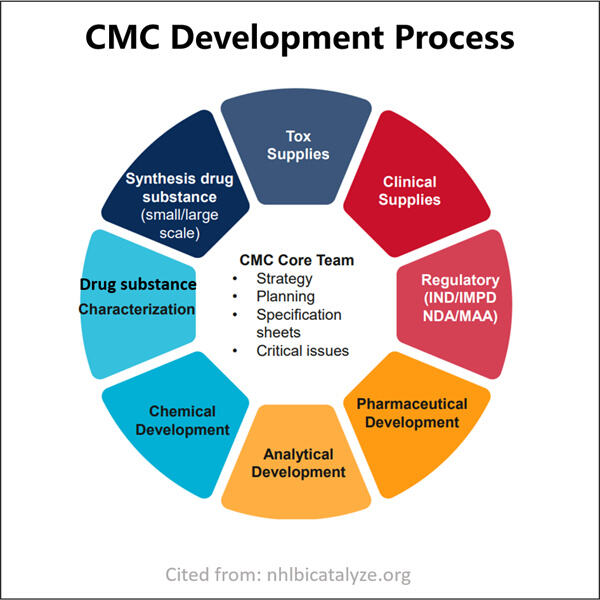
Yaohai Bio-Pharma este un CDMO de avantaj în biologice microbien. Atenția noastră principală a fost orientată spre producerea Secțiunii CMC în Aplicația de Medicament și terapii pentru tratarea animalelor de companie, sănătatea umană și veterinară. Deținem platforme de RD moderne și tehnologie de fabricație care acoperă întregul proces de fabricație, începând cu dezvoltarea liniștilor microbien, bancile de celule, dezvoltarea procesului și a metodelor, până la fabricația comercială și clinică, asigurând livrarea cu succes a soluțiilor inovatoare. În timp, am acumulat o cunoștință vastă despre bio-procesarea bazată pe microbii. Am finalizat cu succes peste 200 de proiecte globale și ajutăm clienții noștri să navigheze prin regulamentele și normele US FDA, EU EMA, Australia TGA, și China NMPA. Datorită experienței și expertizei noastre, putem răspunde repede la cerințele pieței și oferi servicii CDMO personalizate.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN