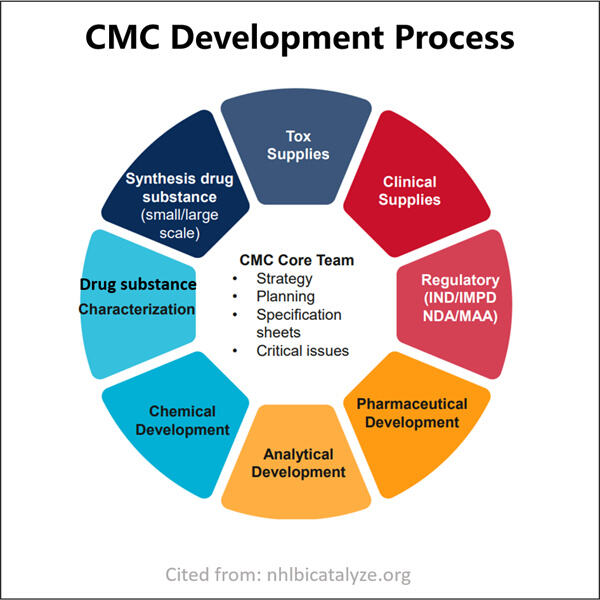
Aanpassing, Efficiëntie & Kosteneffectiviteit
Yaohai Bio-Pharma heeft veel ervaring met biologische producten afkomstig uit microbiele bronnen. We bieden op maat gemaakte RD-oplossingen en productie, terwijl we potentiële risico's minimaliseren. We hebben gewerkt aan verschillende modaliteiten, waaronder recombinante subeen vaccins, peptiden hormonen, cytokines groeifactoren, single-domain antilichamen enzymen, plasmid DNA verschillende mRNA's, en meer. We hebben gespecialiseerd in meerdere microorganismen, inclusief de CMC-sectie in het medicijnverzoek intracellulaire en extracellulaire secretie (opbrengsten tot 15g/L) en intracellulaire oplosbare bacteriën en inclusiebody (opbrengsten tot 10g/L). We hebben ook een BSL-2 fermentatieplatform opgezet om bacteriën-gebaseerde vaccins te creëren. We zijn experts in procesverbetering, verhoging van productopbrengsten en vermindering van productiekosten. We beschikken over een zeer efficiënt technisch team dat garant staat voor punctuele en topkwalitatieve projectaflevering. Dit stelt ons in staat uw unieke producten sneller op de markt te brengen.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN