Kustomisasi, Efisiensi & Hemat Biaya
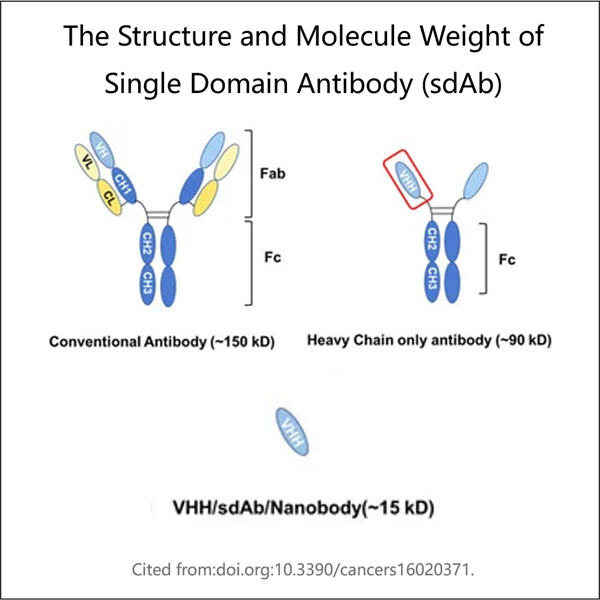
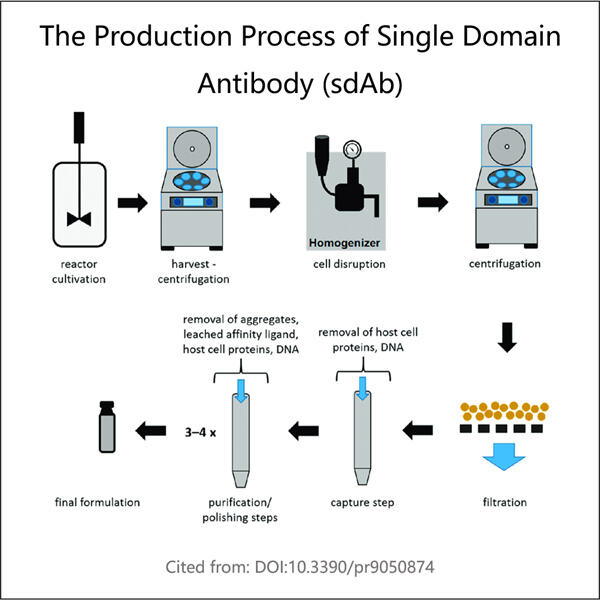
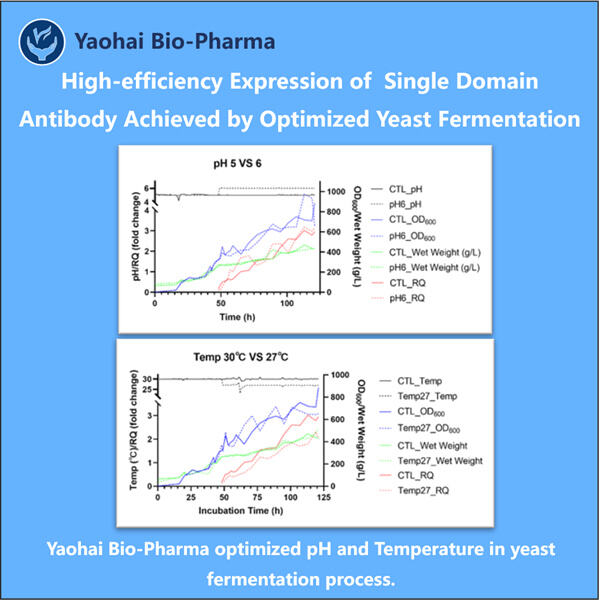
Yaohai Bio-Pharma adalah Pengembangan Proses Antibodi Domain Tunggal (sdAb) dalam biologis berbasis mikroba. Kami menawarkan layanan RD khusus serta solusi manufaktur, sambil meminimalkan risiko. Kami telah terlibat dalam berbagai modalitas seperti vaksin subunit rekombinan, peptida hormon, sitokin faktor pertumbuhan, antibodi domain tunggal, enzim, DNA plasmid, mRNA, dan lainnya. Kami ahli dalam beberapa inang mikroba, seperti ragi ekstraseluler dan intraseluler (hasil hingga 15 gram per liter), sekresi periplasma bakteri serta inklusi tubuh intraseluler larut (hasil hingga 10 gram/L). Selain itu, kami telah mengembangkan platform fermentasi mikroba BSL-2 untuk pengembangan vaksin bakteri. Kami memiliki catatan yang terbukti dalam meningkatkan proses produksi, sehingga meningkatkan hasil dan mengurangi biaya. Dengan tim teknologi yang sangat efisien, kami menjamin pengiriman proyek yang cepat dan andal serta membawa produk Anda lebih cepat ke pasar.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN