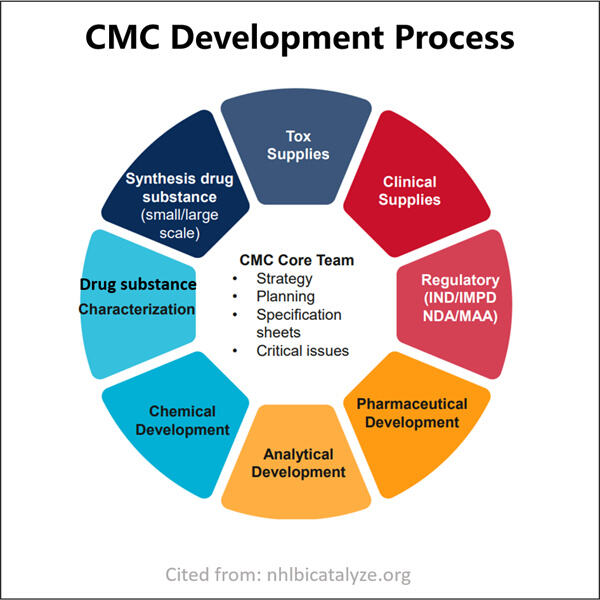
Πλοήγηση στα Τεχνικά Απαιτήματα των Αιτήσεων Φαρμάκων
Αυτό γίνεται επειδή μία από τις πιο βασικές απόψεις της φαρμακευτικής έγκρισης είναι να αποδειχθεί ότι το προϊόν είναι καθαρό και έχει σταθερή αποτελεσματικότητα. Έτσι, ο τρόπος δημιουργίας των φαρμάκων πρέπει να ελεγχθεί ισχυρά, η οποία είναι η λογική για την οποία ορισμένες φαρμακευτικές εταιρείες με σχεδόν παρόμοια μεταβολή s593 έχουν συνεργαστεί για περισσότερα από μια δεκαετία για να παράγουν φάρμακα. Αυτό περιλαμβάνει την ανάγκη για τις εταιρείες να περάσουν μέσω μιας βήματος διαδικασίας για να εξασφαλίσουν ότι το τελικό προϊόν παραμένει σε υψηλά πρότυπα ποιότητας. Αυτό είναι κρίσιμο, καθώς οι ζωές των ανθρώπων είναι σε κίνδυνο από τα φάρμακα που καταναλώνουν.
Οι εταιρείες που καταχωρούν μια φάρμακο-εφαρμογή θα πρέπει να παρέχουν δεδομένα σχεδόν για όλα αυτά που μπαίνουν στο φαρμακευτικό προϊόν και πώς κατασκευάζεται. Αυτό περιλαμβάνει τη χημική σύνθεση, τη διαδικασία κατασκευής και τους παράμετρους ασφάλειας που ενσωματώνονται. Αυτά τα δεδομένα υποστηρίζονται επίσης από επιστημονικά στοιχεία - επιδεικνύοντας ότι το φάρμακο είναι και ασφαλές και αποτελεσματικό. Μιας και η FDA μπορεί να το κατανοήσει καλύτερα πρωτόκολλο Συν-Εγγραφής mRNA φάρμακο, τότε έχουν μεγαλύτερη πιθανότητα να αξιολογήσουν τα δεδομένα του σε σύγκριση με αυτά που έχουν χρησιμοποιηθεί σε άλλες μελέτες (μετα-ανάλυση) σε διαφορετικές περιπτώσεις.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN